GUIA 1
VIRTUAL DE QUIMICA TERCER PERIODO.
GUÍA FÍSICA Y
VIRTUAL DE QUÍMICA GRADO ONCE TERCER PERIODO COLEGIO SAN JOSÉ 2021
PROFESOR. ALIRIO
GUERRERO CHIPAGRA.
CURSOS 1101, 1102 Y
1103.
Estudiantes sin
conectividad (realizar la actividad en hojas blancas o cuadriculadas en carpeta de
papel y entregar en el colegio) (todas las hojas marcadas con el nombre del
estudiante, curso y profesor)
FECHAS LÍMITE PARA LA
ENTREGA:
GUÍAS VIRTUALES
Actividad 1, 2 Y 3
(agosto 12).
Actividad 4 Y
5(septiembre 02).
GUIAS FISICAS
Actividades 1,2,3,4 y
5 (septiembre 02). única entrega.
OBJETIVOS:
- ·Dar razón de la importancia de la química
orgánica para la vida humana
- ·Describir algunas propiedades del carbón y
su importancia en la formación de compuestos orgánicos.
- Formar y dar el nombre a hidrocarburos según
normas de la IUPAC.
METODOLOGÍA.
PRIMERA PARTE
¡Exploremos!
Empecemos el recorrido del estudio de la química orgánica revisando
algunos aspectos y avances de esta ciencia para la humanidad.
RESUMEN:
INTRODUCCIÓN. - La Química Orgánica en la actualidad.
Concepto y origen de la Química Orgánica.
La Química Orgánica se ocupa del estudio de las propiedades y
transformaciones de los compuestos que contienen el elemento carbono. Es llamada
también Química de los compuestos del Carbono.
EXPLOREMOS.
IMAGEN 1 BERZELIUS
En 1806 Jons Jacöb Berzelius introdujo el concepto de química orgánica.
El elevado número y complejidad de estos compuestos se debe a las
características del enlace del carbono, que puede unirse hasta con cuatro
átomos más. El carbono puede formar enlaces estables con muchos átomos
distintos de la tabla periódica y además, puede formar diferentes tipos de
enlaces: simples, dobles o triples. La Química Orgánica, junto con la
Bioquímica, es la ciencia básica que permite explicar los procesos químicos que
tienen lugar en los organismos vivos.
EXPLOREMOS.
La parte más importante de la química orgánica es la síntesis de
moléculas. Los compuestos que contienen carbono se denominaron originalmente
orgánicos porque se creía que existían únicamente en los seres vivos. Sin
embargo, pronto se vio que podían prepararse compuestos orgánicos en el
laboratorio a partir de sustancias que contenían carbono procedente de
compuestos inorgánicos.
En 1828, Friedrich Wöhler consiguió convertir el isocianato de amonio en
urea por descomposición térmica. Así, una sal inorgánica se convirtió en un
producto perteneciente a los seres vivos (orgánico). A día de hoy se han
sintetizado más de diez millones de compuestos orgánicos.
Existe una amplia gama de sustancias (fármacos, plásticos, fibras
sintéticas y naturales, hidratos de carbono, proteínas y grasas) formadas por
moléculas orgánicas. Los químicos orgánicos determinan la estructura de las
moléculas orgánicas, estudian sus reacciones y desarrollan procedimientos para
sintetizar compuestos orgánicos. Esta rama de la química ha afectado
profundamente a la vida en los siglos XX y principios del XXI: ha perfeccionado
los materiales naturales y ha sintetizado nuevas sustancias que han mejorado la
salud, aumentado el bienestar y favorecido la utilidad de los productos
empleados en la actualidad.
IMAGEN 2 PRODUCTOS SINTETICOS
Tipos de plásticos.
Toda la IQO (industria química orgánica) se alimenta de las industrias
químicas pesadas cuyas materias primas son el petróleo, el gas natural y el
carbón. Otra gran parte de la IQO se abastece de productos naturales de origen
animal o vegetal. Los productos obtenidos en la IQO se utilizan bien como
intermedios para otros procesos industriales o bien para consumo directo
(fármacos, plásticos…). Estos últimos, es decir, los productos orgánicos
industriales utilizados para consumo directo pueden englobarse en dos grandes
grupos: - Aquellos que se producen a gran escala, toneladas por año, y su
precio por kilogramo es moderado. Como son los plásticos, abonos, detergentes,
plaguicidas… - Aquellos que se fabrican en cantidades pequeñas, pero su precio
es muy alto y, por tanto, el volumen de sus ventas, en dinero, también lo es.
La fabricación de estos productos constituye la llamada Industria Química
Orgánica fina. La IQO final en la actualidad es la IQO que posee mayor
competencia, mayor gasto en investigación y mayor velocidad de cambio.
IMAGEN 3 FUENTES DE ENERGIA
SECTORES DE LA INDUSTRIA QUÍMICA ORGÁNICA
IMAGEN 4 INDUSTRIA QUIMICA ORGANICA.
Texto recuperado de:
https://www.repositoriodigital.ipn.mx/bitstream/123456789/15211/6/introduccion.pdf
EL ÁTOMO DE CARBONO EN LA QUÍMICA ORGÁNICA.
ACTIVIDAD 1.
a.
Realice un resumen de la importancia de la química orgánica para la
vida humana y para el medio ambiente. (cita las fuentes bibliográficas)
b.
Haga una lista de cinco científicos de la química orgánica, el aporte
realizado a esta ciencia y la época.
c.
Revise los productos de aseo y otros materiales que estén
disponibles en tu casa, nombrarlos y registrar los materiales de los que están
hechos.
d.
Resuma en qué campos de la vida humana interviene la química orgánica y
de qué manera. (Cite las fuentes bibliográficas)
¿QUÉ ES EL ÁTOMO DE
CARBONO?
El carbono es el
elemento mayoritario en la Tierra, y esencial para la vida. Es el componente principal de la materia orgánica; también integra el producto
final dióxido de ca del metabolismo de la mayoría de los seres vivos y del proceso de combustión: el dióxido de carbono se presenta bajo numerosas estructuras y también de
manera amorfa; sus propiedades físicas son a menudo muy contrastantes.
Tiene la propiedad de poder combinarse con casi todos los elementos
se puede combinar tanto con metales y no metales (ejemplos:
carburo de calcio, disulfuro de carbono, cloroformo, etc.).
Se calculan aproximadamente
unos 10 millones de compuestos de carbono, siendo muchos de ellos
esenciales para la vida en el planeta.
A continuación, a
modo de resumen, las características y propiedades del carbono.
IMAGEN 5 EL CARBONO
CARACTERÍSTICAS DEL
ÁTOMO DE CARBONO:
Número atómico 6 y
número de masa 12
Esto significa
que tiene en su núcleo 6 protones y 6 neutrones, y que dicho núcleo está
rodeado por 6 electrones. Esos electrones se distribuyen en su estructura de la
siguiente manera: dos en su primer nivel (llamado s) y cuatro en su
segundo nivel (llamado p)
Es
tetravalente, Esto significa que, como se señaló, tiene 4 electrones
orbitando en su último nivel de energía, los cuales se pueden combinar con los
electrones más externos de otros átomos, a menudo también de carbono, formando enlaces covalentes.
Tres posibles
hibridaciones
En virtud de esos
cuatro electrones de la capa más externa que se pueden combinar con los
electrones de otros átomos, el átomo de carbono puede formar tres tipos de
uniones, las que tienen implicancias en la geometría molecular final. Estos
enlaces pueden ser: simples (hibridación sp3), dobles (hibridación sp2) Y
triples (hibridación sp)
Fuente: https://www.caracteristicas.co/atomo-de-carbono/#ixzz6wYjI0m5Z
IMAGEN 7. TIPOS DE
HIBRIDACION
Como ya hemos estudiado, el carbono es un elemento muy importante para
los seres vivos pues hace parte de todas las biomoléculas como grasas,
azúcares, grasas, proteínas y ácidos nucleicos entre otras.
El carbono, se halla en la naturaleza en sus formas alotrópicas
(diamante, grafito, fullerenos, nanotubos y carbonos.
Los átomos de
carbono, tienen la propiedad de unirse entre sí para formar cadenas rectas y
ramificadas que pueden ser abiertas o cerradas, con enlaces simples, dobles y
triples. En el caso de los hidrocarburos, los átomos de
carbono sólo están unidos a átomos de hidrógeno. . Sin embargo, también pueden
formar enlaces covalentes con átomos de otros elementos como el
oxígeno y el nitrógeno formando parte de un grupo funcional. Dependiendo del
arreglo de los átomos los grupos funcionales reciben un nombre.
Funciones químicas orgánicas
Una función química es un grupo o familia de compuestos que
tienen propiedades semejantes debido a que en su composición tienen un átomo o
grupo de átomos característicos llamado grupo funcional.
El grupo funcional es un átomo o grupo de átomos que define la
estructura de una familia determinada de compuestos orgánicos y también define
sus propiedades. • Las principales funciones químicas orgánicas son: alcoholes,
éteres, aldehídos, cetonas, ácidos carboxílicos, aminas, ésteres, amidas,
anhídridos de ácido.
Estas son algunas de las funciones químicas que forman el átomo de
carbono.
A continuación, se presenta un cuadro con las clases de compuestos o
funciones químicas orgánicas que poseen al carbono como elemento principal.
IMAGEN 8
. FUNCIONES QUIMICAS ORGANICAS
IMAGEN 9
LOS HIDROCARBUROS.
LOS HDROCARBUROS
El átomo de carbono forma una gran variedad de compuestos llamados
hidrocarburos,
Como se aprecia en el cuadro, los hidrocarburos se clasifican en
alifáticos (alcanos, alquenos y alquinos) y los aromáticos (benceno y sus derivados)
GEOMETRÍA DE LOS HIDROCARBUROS
Dependiendo de la clase de hidrocarburos, los ángulos de enlace entre
los átomos de carbono varían haciendo que las moléculas adquieren una forma
tridimensional que es responsable de crear la estructura de la materia
orgánica; no solo las funciones químicas orgánicas sino también las
biomoléculas que forman a los seres vivos.
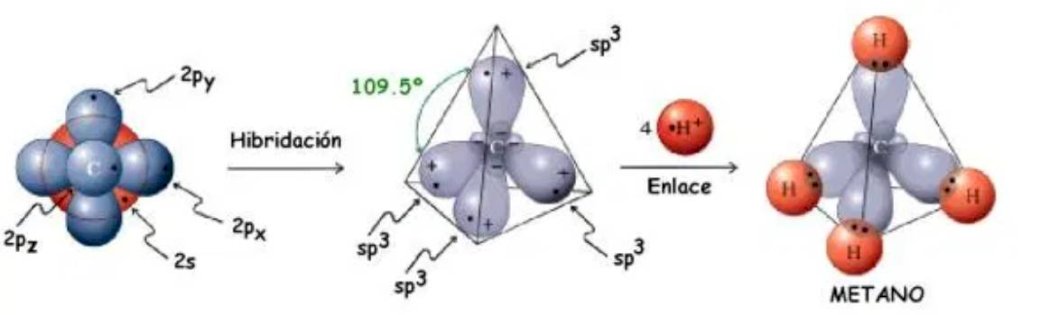
FORMA GEOMÉTRICA DE
LAS MOLÉCULAS CARBONADAS SEGÚN EL TIPO DE HIBRIDACIÓN PRESENTE.
OMAGEN 10 IMAGEN DE
ORBITALES HIBRIDOS.
RECUPERADO DE https://www.textoscientificos.com/quimica/organica/hibridacion-carbono
ACTIVIDAD 2. Resume los siguientes aspectos.
a. ¿Cuántos electrones de valencia posee el átomo
de carbono?
b. ¿Qué clases de enlaces químicos forman el
carbono con otros carbonos y con otros elementos como el hidrógeno?
c. ¿Cuántos enlaces forma el carbono en estado
excitado?
d. ¿Qué es la hibridación del carbono? ¿Cuántas
clases de hibridación existen y en qué se diferencian?
e. Dibuje una molécula en cada estado de hibridación
que contenga mínimo dos átomos de carbono
f. ¿Qué hibridación presenta en los compuestos
alquenos?
g. ¿Qué hibridación presenta el carbono en
los compuestos alquinos?
h. Dibuje una molécula para un
compuesto alcano, un alqueno y un alquino conservando los ángulos de enlace
según el tipo de hibridación que posean.
ACTIVIDAD 3.
Utilizando los conceptos y ejemplos trabajados, realice la representación
tridimensional en material reciclable de una molécula de hibridación SP, una en
SP2 y una en SP3. (señale en cada una los ángulos de enlace carbono a carbono,
el tipo de enlace sigma o pi y la clase de hidrocarburo al que pertenece)
SEGUNDA PARTE
NOMENCLATURA DE HIDROCARBUROS
En esta unidad didáctica denominada “hidrocarburos “tema relacionado al
estudio del carbono y sus capacidades para formar grandes cadenas de carbono,
se abordarán conceptos y normas que permiten identificar y reconocer diferentes
clases de hidrocarburos su importancia y nomenclatura. La temática presentada
es algo extensa por tanto se realizará una primera sesión con conceptos
generales
ACTIVIDAD 4.
Realice la lectura
del texto, consulte otros artículos relacionados y resuelva la actividad.
¿SABES QUÉ TIPO DE
COMBUSTIBLE SUSTITUIRÁ AL PETRÓLEO CUANDO SE ACABE? ¿Qué puede sustituir al oro
negro? Los científicos insisten en que las reservas mundiales de petróleo no
son eternas, por tanto, hay que buscar otras alternativas. El petróleo se ha
convertido en un combustible imprescindible en nuestras vidas, aunque no por
ello insustituible, pues algún día se terminará, es por ello que muchos
científicos están tratando de hallar a su sustituto. Filip Rutberg, académico,
director del Instituto de Electrofísica y Energía Eléctrica de la Academia de
Ciencias de Rusia, opina que el petróleo, gas y carbón no seguirán siendo las
principales fuentes de energía de la humanidad más allá de la primera mitad del
siglo XXI. “Hay muchos yacimientos de carbón en el mundo, pero si no se procesa
en gas por medio una tecnología específica, se puede arruinar el planeta solo
con la combustión de carbón. ¿Qué queda?”, pregunta el experto. “Es posible que
los hidrocarburos sean reemplazados por la energía de fusión, pero este tema no
se resolverá pronto: hay retos tecnológicos asociados con problemas puramente
científicos”, agregó. “La energía alternativa va a ganar posiciones: fuentes
renovables como la solar, eólica, geotérmica, etc. De acuerdo con diversas
estimaciones, dentro de 20-30 años la cuota mundial será del 12% al 15%. En
Brasil y en el estado de California (EE.UU.) ahora casi todos los coches operan
con combustible líquido artificial producido a partir de caña de azúcar y maíz.
Estas tecnologías están evolucionando rápidamente: los biocombustibles de
tercera generación se producen a partir de algas cultivadas a escala comercial”
http://www.portalminero.com/pages/viewpage.action?pageId=89620513
¿Cuáles son los
principales hidrocarburos usados como fuente de energía?
¿Cuáles son las
nuevas fuentes de energía para la humanidad?
¿Qué opinas acerca de
que las grandes industrias de las energías fósiles no invierten en nuevas
fuentes de energía?
EXPLOREMOS
observa con atención:
https://www.youtube.com/watch?v=0xE-CCGBSjs
LOS HIDROCARBUROS.
La habilidad que
tiene el carbono de formar uniones covalentes con otros átomos de carbono y con
átomos de hidrógeno conduce a la formación de compuestos muy estables. Los
compuestos que solo contienen los elementos carbono e hidrógeno son
denominados hidrocarburos. Estos hidrocarburos pueden extraerse de los
yacimientos de petróleo y gas natural, "el petróleo y sus derivados”. Ambos
combustibles son mezclas de hidrocarburos. ¿Cómo se pueden clasificar los
hidrocarburos?
El estudio de la
gran cantidad de compuestos orgánicos se simplifica si se considera que están
formados por un fragmento hidrocarbonado y un grupo de átomos que controlan la
reactividad de la molécula. Este fragmento puede incluir o no otros elementos diferentes
al carbono e hidrógeno, como por ejemplo oxígeno, nitrógeno, azufre, fósforo,
algún halógeno o incluso combinaciones de estos unidos entre sí o con el
carbono. A este grupo de átomos se lo denomina grupo funcional.
Este grupo
funcional les otorga características particulares a los compuestos que lo
contienen y es posible considerar a todas las moléculas que contienen el mismo
grupo funcional como una familia. A estas familias se las denomina series
homólogas. Una serie homóloga es un grupo de compuestos que tienen el mismo
grupo funcional y, por lo tanto, presentan propiedades químicas similares y
propiedades físicas que varían gradualmente a medida que aumenta el número de
átomos de carbono en la cadena. Por ejemplo: el etano y el propano pertenecen a
la misma serie homóloga. Se los puede representar de distintas maneras, como
puede observarse a continuación:
• Mediante la
fórmula molecular: indicando la cantidad de carbonos e hidrógenos que forman
una molécula. Ejemplo:
C2H6, etano
C3H8, propano
• Mediante la
fórmula semidesarrollada: en ella se indica cómo los átomos de carbono e
hidrógeno están agrupados. Ejemplo:
CH3CH3,
etano CH3CH2CH3, propano
• Mediante la
fórmula de esqueleto: en ella los átomos de carbono se representan como los vértices
de segmentos de líneas que representan la unión entre átomos de carbono. Se
supone que cada átomo de carbono está unido a la vez a tantos átomos de
hidrógeno como sea necesario para que tenga cuatro enlaces en total (los átomos
de hidrógenos se omiten en este tipo de fórmulas). Otros átomos distintos del C
y el H o grupos radicales (R) deben escribirse de modo explícito. Ejemplo:
• Mediante
diagramas de bola: en ellos los átomos de los diferentes elementos están
representados por esferas de diferente diámetro y las uniones por palitos.
Los programas de
representación de moléculas ayudan a visualizar estas diferentes formas
de representación (por ejemplo,
En el caso de los
hidrocarburos, dependiendo de si las uniones entre carbonos son simples, dobles
o triples, y contengan o no anillos (estructuras cíclicas) se pueden mencionar
varias series homólogas que se resumen en la siguiente tabla:
IMAGEN 11 TABLA DE
HIDROCARBUROS
Tabla 1.
Hidrocarburos
|
Hidrocarburo
|
Tipo de unión entre
carbonos
|
Ejemplo
|
Fórmula general
|
El nombre termina
en
|
Sitio para visualizarlos
|
|
Alcanos
|
Simple
|
C2H6
etano
|
CnH2n+2
|
-ano
|
alcanos lineales
|
|
Alquenos
|
Doble
|
C2H4
eteno
|
CnH2n
|
-eno
|
Alquenos
|
|
Alquinos
|
Triple
|
C2H2
etino
|
CnH2n-2
|
-ino
|
Alquinos
|
|
Ciclo
alcanos
|
Simple y anillo
|
C6H12
ciclo hexano
|
CnH2n
|
-ano
|
Cicloalcanos
|
|
Aromático
|
Simple y doble,
anillo
|
C6H6
benceno
|
-
|
Como derivado del
benceno
|
Hidrocarburos aromáticos
|
ALCANOS, ALQUENOS Y ALQUINOS.
Veamos cerca de los
alcanos
https://www.youtube.com/watch?v=yzKev2SWIpY
Veamos acerca de
los alquenos
https://es.coursera.org/lecture/qimica-carbono/que-distingue-a-los-alquenos-WCwAq
Veamos acerca de
alquinos
https://www.alonsoformula.com/organica/alquinos.htm
ACTIVIDAD
5.
1.
Consulta todas las normas de nomenclatura de hidrocarburos y con las
explicaciones dadas en los videos asigne el nombre a cada una de las siguientes
moléculas
·
CH3 – CH3
·
CH3 – CH2 – CH3
·
CH3 – (CH2)3- CH3
·
CH3 – CH2- CH2 – CH2 – CH2 – CH3
·
CH2 = C H - CH2 - CH3
·
CH3 – CH2 – CH – CH = CH – CH3
·
CH3 – CH – CH2 – CH2 – CH2- CH2 – CH2- CH2 – CH2 – CH3
·
CH3- CH2 – CH2 – CH = CH – CH2 – CH = CH – CH3
·
CH3 – (CH2) 10 CH2 – CH = CH – CH3
2.
Construya las moléculas de los siguientes compuestos:
·
ciclo propano.
·
3,3,4 – trimetil un decano
·
metilciclopentano
·
3- octino
·
2,5 –heptadieno
·
3 – metil 4 octino
·
1,3,5 ciclohexatrieno
·
tetracloroetano
·
benceno
·
antraceno
·
ciclopentanoperhidrofenantreno